RECUENTO DE CÉLULAS EN CÁMARA DE NEUBAUERCÁLCULO DE RESULTADOS Y CASOS
Recuento celular:
Es la determinación total de número de células sanguíneas como hematíes leucocitos y plaquetas por unidad de volumen sanguíneo, se puede realizar por métodos automatizados o por métodos manuales utilizando cámara de Neubauer.Principios y características de cámara de Neubauer
Es una placa base rectangular y gruesa de vidrio óptico especial, del tamaño de un portaobjeto, en el tercio medio se hallan cuatro ranuras fresadas longitudinales que transcurren en paralelo con respecto a los laterales cortos. Las dos superficies laterales más grandes están sin trabajar y sirven para la rotulación, el puente central y los dos puentes exteriores están rectificados planos y pulidos, la superficie del puente central es más profunda que los dos puentes exteriores, el puente central conocido como la profundidad de la cámara de neubauer están grabadas las redes o retículos grabados con diamante para el recuento de las partículas como células o elementos formes.Cámara de neubauer:
La cámara de Neubauer se utiliza para determinar el número de células por unidad de volumen de un líquido, ejemplo: la cantidad de leucocitos, eritrocitos y plaquetas en un volumen de sangre u otras partículas como bacterias esporas del moho y cualquier tipo de recuento citológico, en suspensiones bajo el microscopio. Las células de nuestro interés se encuentran visualmente con un microscopio, la cámara de Neubauer o cámara de cuenta glóbulos, hematímetro o hemo- citómetro presenta un porta objeto de vidrio grueso, lleva grabadas en su superficie tres prismas paralelos, el prisma central está dividido en dos por un surco transversal y sobre dos mitades se ha trazado los retículos. Los prismas laterales están ligeramente elevados con una altitud de 0.1mm con respecto al prima central y el cubre objeto, el cubreobjeto y en donde se colocan la muestra diluida para efectuar el recuento.El cubre hematímetro es un vidrio más delgado que se coloca sobre las primas laterales, en la imagen 1 se visualiza en corte longitudinal de como se ve la cámara Neubauer una vez colocado el cubrehematímetro o lámina cubre cámara propiamente dicho. Es así que existe una distancia de 0.1mm entre el cubre hematímetro y el prisma central donde están grabado el hematímetro que nos permite hacer el recuento de células de nuestro interés, presente en una muestra diluida ya sea en sangre, líquidos biológicos en una solución en el espacio que hay entre el prisma central de cámara de Neubauer y el cubre hematímetro se vamos a denominar la profundidad de volumen mm3.
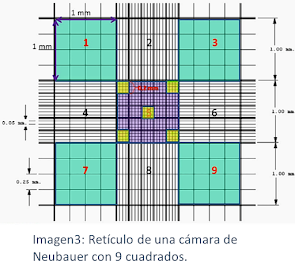
Cuando se observa los retículos los retículos cuadriculados en microscopio se observa los 9 cuadrados y cada cuadrado tiene sus subdivisiones; cada uno de los nueve cuadrados grandes tiene una medida de 1mm de largo y 1mm de ancho, por lo que cada uno tiene una superficie de 1mm2. Los cuatro 4 cuadrados grandes de esquina señaladas
por los números 1, 3, 7 y 9 se utiliza para el recuento de leucocitos y espermatozoides, para realizar el contaje de dichas células se le debe realizar una dilución, es decir en un líquido Turk para los leucocitos.
De la misma forma el cuadrado central (5), está dividido en 25 (1, 2, 3, 4…25) cuadrados medianos, con aristas de 0.2mm y estando cada cuadrado mediano subdividido en dieciséis (16) cuadrados pequeños con aristas de 0.05mm; en cuadrado central se hace el recuento de eritrocitos, plaquetas y levaduras, contando los 5 cuadrados pequeños como se observa en la (figura 3).
Procedimiento en el recuento de leucocitos en cámara de Neubauer
Para el contaje de leucocitos se debe tener la muestra de sangre anticoagulada con EDTA (Etilendiaminotetraacético) en forma de sales sódica y potásica. El líquido de Turk para diluir la sangre es hipotónica lo que provoca la hemolisis de eritrocitos para que no interfiera en el recuento de leucocitos, el líquido de Turk consta de 2 mL de ácido acético glaciar, 1mL de genciana al 1% y agua destilada como solvente para 1000mL de solución.Para hacer la dilución de sangre con el líquido de Turk en una proporción de 1 en 20 (1/20), es realizar con la pipeta de Thoma, el cual consiste en un tubo de vidrio del fondo blanco graduado en una escala de 11 subdivisiones iguales y que presenta un bulbo central, con una pequeña perla blanca en su interior, cada pipeta requiere una aspiración con un tubo de goma o pipeta de aspiración.
En primer lugar se llena la pipeta de Thoma con sangre hasta la marca de 0,5 volúmenes, luego se limpia con una gaza o papel toalla el excedente de la sangre, posteriormente se introduce la pipeta de Thoma a la solución de Turk previamente separada para evitar la contaminación para evitar la contaminación al líquido, se absorbe hasta llegar a la marca de 11 volúmenes, no se debe dejar burbujas en este proceso porque puede alterar el recuento y la dilución; si fuese así volver a cargar siguiendo las paso ya mencionados.
Se tapa a ambos extremos con un Parafilm o con la mano luego se coloca en rotor automático o se hace manualmente, de 2 a 3 minutos. Con este procedimiento se realiza una dilución 1 en 20; ¿Por qué dilución 1 en 20?, es debido a que el 0,5 volumen de sangre se diluye en un volumen total de 10 volúmenes, sigo sin entender y pensaran ¿por qué no 1 en 11? Lo que pasa es que cuando terminamos de llenar hasta la marca de 11 volúmenes, desde la punta de pipeta hasta la marca de 1 volumen solo hay liquido de Turk, ya que la real dilución de la sangre ocurre en el bulbo, por lo que a 11 se le resta 1 volumen quedando como 10 volúmenes en total, eso quiere decir que el 1 volumen de sangre se está diluyendo en un volumen total de 20 volúmenes. Analizando con un método matemático simple llegamos que:
Si 0,5 volumen____________________se diluye en un volumen total de 10 volumenes
1 volumen___________________________________ de sangre en cuanto se diluiria?
(1 x 10)/(0,5)=20
Entonces la dilución seria 1 en 20.
Si 20 uL de sangre____________________se diluye en un volúmen total de 400 uL
1 volumen___________________________________ de sangre en cuanto se diluiria?
(1 x 400)/(20µL )=20
Entonces la dilución sería 1 en 20.
El siguiente paso es cargar a la cámara de neubauer la sangre diluida en la solución de Turk, para ello se emplea una pipeta automática o un capilar; si la dilución se hizo en una pipeta de Thoma se carga directamente pero antes sacar unas 4 gotas antes de llenar a la cámara de Neubauer, así de esta manera la dilución se distribuye en el hematímetro y cubrehematímetro por acción de la capilaridad en el espacio de 0,1mm de profundidad. La cámara de Neubauer consta de 2 hematímetro usualmente en la práctica clínica diaria uno de ellos se utiliza para el recuento de leucocitos de un paciente y el otro retículo para el otro paciente, dejar reposar en una cámara húmeda por 2 o 3 minutos para luego colocar en un microscopio para poder observar hematímetro las células o leucocitos que se encuentran distribuidas.
Observación de leucocitos en microscopio
Cuando colocamos la cámara de Neubauer en el microscopio se observa los retículos cuadriculados y que también sabemos que el conteo de leucocitos se hace en los cuatro (4) cuadrados de las esquinas (1, 3, 7 y 9), los cuales tienen 1mm x 1mm de superficie 1mm2. Cuando se observa en el microscopio la cámara de Neubauer la dilución con el líquido de Turk se observa las células y el contaje se hará en el sentido zig zag siguiendo en sentido de la flecha sin levantar los ojos del microscopio, se contará todas las células que se ubican en los cuadrados mencionados teniendo en cuenta e incluyendo el recuento de las células que se encuentran sobre las líneas.Por ejemplo, en el cuadrado 1 contamos 20 células, en el 3er cuadrado 23 células, en 7 también 23 leucocitos y en 9 contamos 21 leucocitos; obteniendo 87 leucocitos quiere decir que hay 87 células en 4mm2 ya que cada cuadrado tiene 1mm x mm y como existe una altura de 0,1mm del prisma medio hacia el cubre objeto entonces el volumen total es 4mm2 x 0,1mm igual 0,4mm3, entonces tenemos 87 leucocitos en un volumen de 0,4 mm3.
Ahora calculemos el factor de estándar para el conteo de leucocitos; esto será igual a la superficie por la altura es igual a 0,4 mm3 entonces aplicamos análisis matemático simple:
Si N leucocitos ____________________se contaron en un volumen total de 0,4mm3
En un volúmen de 1mm3 cuantas celulas habrán ____________________________?
Multiplicamos lo siguiente para hallar el factor: 1mm3 x dilución (20) dividido entre volumen (0.4mm3)
Número de células /〖mm〗^3= 50
entoces el factor es 50; ahora para hallar el recuento total de leucocitos multiplicamos el factor por el numero de celulas contadas(N).
Número de células/〖mm〗^3=50 x 87
Obtenimos 4,350 leucocitos por mm3 o es lo mismo decir 4,350/uL
Otra fórmula para deducir el factor para el recuento de leucocitos:
Recuento de GB = N x 50
Recuento de GB = 87 x 50 = 4.350 leu/mm3
Qué pasa si al hacer una dilución 1/20 y al observar en el microscopio observamos una cantidad mayor, células sobrepuestas y que no deja el recuento real. Ejemplo en los pacientes con leucocitosis, es tan grande el número de células y el contaje se dificulta como consecuencia error al contar y reporte con margen de error mayor a lo habitual. ¿qué hacer? La respuesta sería hacer una dilución mayor, entonces ¿Cómo hacer una dilución que deseamos?, ejemplo 1/100, que es mucho mayor que el 1/20. Para ello realizamos lo siguiente: escoger un volumen de sangre para diluir, en este caso 20uL de sangre total luego lo multiplicamos el volumen de sangre por la dilución, (20uL x 100 = 2000uL) y esto sería el volumen final(2000uL) luego vamos a restar al volumen total el volumen de sangre (2000ul – 20uL = 1980uL) quiere decir que el 1980 es el volumen del diluyente, el líquido de Turk, entonces se hace para hacer una dilución 1/100 colocando 20uL de sangre con 1980uL de diluyente Turk y luego se realiza los mismos pasos de cargar la dilución en la cámara de Neubauer y observamos en el microscopio la densidad leucocitaria ha disminuido y el cual se podría decir que se puede contar leucocitos.
CAPÍTULO II
RECUENTO DE ERITROCITOS EN CÁMARA DE NEUBAUER
Para el contaje de eritrocitos se debe tener la muestra de sangre anticoagulada con EDTA (Etilendiaminotetraacético) en forma de sales sódica y potásica. El líquido de Hayem, SSF para diluir la sangre es isotónica lo que provoca la hemólisis de leucocitos para que no interfiera en el recuento de eritrocitos.Para hacer la dilución de sangre con el líquido de Hayem en una proporción de 1 en 200 (1/200), es realizar con la pipeta de Thoma, el cual consiste en un tubo de vidrio del fondo rojo graduado en una escala de 101 subdivisiones iguales y que presenta un bulbo central, con una pequeña perla roja en su interior, cada pipeta requiere una aspiración con un tubo de goma o pipeta de aspiración.
En primer lugar se llena la pipeta de Thoma con sangre hasta la marca de 0,5 volúmenes, luego se limpia con una gaza o papel toalla el excedente de la sangre, posteriormente se introduce la pipeta de Thoma al diluyente en este caso el Hayem previamente separada para evitar la contaminación, se absorbe hasta llegar a la marca de 101 volúmenes, no se debe dejar burbujas en este proceso porque puede alterar el recuento y la dilución; si fuese así volver a cargar siguiendo las paso ya mencionados.
Se tapa a ambos extremos con un Parafilm o con la mano, luego se coloca en rotor automático o se hace manualmente de 2 a 3 minutos. Con este procedimiento se realiza una dilución 1 en 200; ¿Por qué dilución 1 en 200?, es debido a que el 0,5 volumen de sangre se diluye en un volumen total de 100 volúmenes, ustedes pensarán ¿por qué no 1 en 101? Lo que pasa es que cuando terminamos de llenar hasta la marca de 101 volúmenes, desde la punta de pipeta hasta la marca de 1.0 volumen solo hay diluyente, ya que la real dilución de la sangre ocurre en el bulbo, por lo que a 101 se le resta 1 volumen quedando como 100 volúmenes en total, eso quiere decir que el 1 volumen de sangre se está diluyendo en un volumen total de 200 volúmenes. Analizando con un método matemático simple llegamos que:
Si 0,5 volumen____________________se diluye en un volumen total de 101 volumenes
1 volúmen___________________________________ de sangre en cuanto se diluiria?
(1 x 100)/(0,5)=200
Entonces la dilución seria 1 en 200.
Observación de eritrocitos en el microscopio
Cuando colocamos la cámara de Neubauer en el microscopio se observa los retículos cuadriculados y que también sabemos que el conteo de eritrocitos se hace en 5 cuadrados medianos del centro (a, b, c, d y e), los cuales tienen una superficie 0,4mm2 (0,2 x 0,2 =0,4). Cuando se observa en el microscopio la cámara de Neubauer en la dilución se observa las células y el contaje se hará en el sentido zig zag siguiendo en sentido de la flecha sin levantar los ojos del microscopio, se contará todas las células que se ubican en los cinco cuadrados centrales mencionados, teniendo en cuenta e incluyendo el recuento de las células que se encuentran sobre las líneas en forma de L.Por ejemplo, en el cuadrado (a) contamos 90 células, en el (b) cuadrado 93 células, en (c) también 92 leucocitos, en (d) contamos 91 y en (e) contamos (94) eritrocitos; obteniendo 460 eritrocitos, quiere decir que hay 460 células en 0,04mm2 ya que cada cuadrado tiene 0.2mm x 0,2mm y como existe una altura de 0,1mm del prisma central de la cámara de Neubauer hacia el cubre objeto entonces el volumen total es 0.2mm2 x 0,1mm igual 0,02mm3, entonces tenemos 460 eritrocitos en un volumen de 0,02 mm3.
Ahora calculemos el factor de estándar para el conteo de eritrocitos; esto será igual a la superficie por la altura es igual a 0,02mm3 entonces aplicamos análisis matemático simple:
Si N eritrocitos ____________________se contaron en un volúmen total de 0,02mm3
En un volúmen de 1mm3 cuantas células habrán ____________________________?
Multiplicamos lo siguiente para hallar el factor: 1mm3 x dilución (200) divido por volumen(0.02mm3)
Número de células /mm3= 10,000
Entoces el factor es 10,000; ahora para hallar el recuento total de eritrocitos multiplicamos el factor con el número de células contadas(N).
Número de células/〖mm〗^3=10,000 x 460
Obtenimos 4,600 000 eritrocitos por mm3 o es lo mismo decir 4,600 000/mm3 = (4,6 x 106)cel/uL
Otra fórmula para deducir el factor de dilución para el recuento de eritrocitos haciendo la inversa de:
Recuento de GR=N (5 x 0,04〖mm〗^2 ) 1/10 x (0.5)/100
Recuento de GR=N x 4 x 1/10 x (0.5)/100 x 2
Recuento de GR=N x 4 x 1/10 x 1/200
Recuento de GR = N x 10,000
Recuento de GR = 460 x 10,000 = 4.600 000 erit./mm3
Otra forma de calcular el recuento de leucocitos es aplicando esta fórmula que también esta aceptado universalmente.
Hallando la fórmula llegaremos a la misma cantidad de eritrocitos contados por mm3
CAPÍTULO III
RECUENTO DE PLAQUETAS EN CÁMARA NEUBAUER
Las plaquetas circulantes son células inactivas en forma de disco, con superficies lisas, después de una lesión se produce cambios que afecta su morfología y bioquímica activándolas, las cuales son capaces de crear un tapón hemostático primario. Las plaquetas en forma de disco se transportan en protrusiones filamentosas largas y delgadas lo cual sugiere contracción activa, la adherencia de plaquetas en si la agregación, se presenta normalmente en la hemostasia, pero también en trombosis, pueden producir in vitro, activándose por las sustancias químicas conocidas como ATP, adrenalina, serotonina, ácido araquidónico y trombina, ellos participan tanto en la hemostasia primaria como en secundaria, es decir en el proceso de la coagulación.El megacariocito es células madres que forman parte de las células hematopoyético en la medula osea y en otros tejidos, se trata de una célula muy grande con un 30 µm de diámetro y la participación de megacariocito en la hematopoyesis se limita la producción de plaquetas o trombocitos. Para formar las plaquetas los megacariocitos liberan fragmentos de su citoplasma directamente a un bazo sinusoide, es decir, un bazo poroso transportando así a la circulación sanguínea.
Para poder entender el uso de la cámara de Neubauer y el recuento de plaquetas primero saber las dimensiones de la cámara, necesitamos sangre anticoagulada con EDTA, solución de oxalato de amonio al 1%, es decir un gramo de oxalato de amonio por cada 1000 mL de solución; o es lo mismo 10 gramos de oxalato de amonio por cada litro de solución.
Para hacer la dilución con oxalato de amonio y posteriormente hacer conteo de plaquetas en cámara de Neubauer se trabaja de la siguiente manera:
Agregar 1,98 mL (1980µL) de solución de oxalato de amonio en un tubo de ensayo, luego con la ayuda de una pipeta automática se agrega 0.02mL (20µL) de sangre total, mezclar y se deja reposar para que lisen a los eritrocitos que pueden interferir en el recuento, haciendo esta dilución obtenemos 2mL que es el volumen total. Aplicando análisis matemático simple hallamos el factor de la dilución.
Si 20µL de sangre ____________________se diluye en un volumen total de 2000µL
1 volúmen___________________________________ de sangre en cuanto se diluiria?
(1vol x 2000µL)/(20µL)=100vol
Entonces la dilución seria 1 en 100.
Se monta la cámara de Neubauer con ayuda de una pipeta automática y dejar en el reposo por 10 minutos en una cabina húmeda para que la muestra cargada en la cámara de Neubauer no se seque, en este proceso las plaquetas se sedimentan en fondo y mejora la visualización y el contaje; la cámara húmeda consiste en una placa Petri con un papel de filtro humedecido con agua destilada.
Posteriormente se lee con el objetivo de 40x contando las plaquetas; si se compara el tamaño de las plaquetas con los leucocitos, es evidente que las plaquetas son más pequeñas que el leucocito (7 – 15 µm de leucocitos y 2 – 3 µm de plaquetas). Con solución de oxalato de amonio en el microscopio las plaquetas se observan como corpúsculos redondeados de tamaño relativamente pequeño y muy refringentes, procurar no confundir con restos eritrocitarios sobre todo con partículas de polvo. Para el contaje de plaquetas se usa el cuadrado central, este cuadrado central tiene 1mm x mm = 1mm2 de superficie, existe muchos protocolos de contaje plaquetario.
Primer protocolo de recuento de plaquetas
Sabemos que las dimensiones del cuadrado central de una cámara de Neubauer; son en total 25 cuadrados medianos a su vez cada cuadrado mediano esta subdividido en 16 cuadrados pequeños, el cuadrado mediano tiene una medida de 0.2mm x 0.2mm como superficie de 0.04mm2; uno de los protocolos que se usa con más frecuencia consiste en contar los 5 cuadrados medianos al igual que los eritrocitos y multiplicamos por 5. Entonces, la superficie total de contaje es 0.2mm2 (superficie: 0.04mm2 x 5 =0,02mm2), ahora calculemos el factor de estándar del contaje de plaquetas bajo a estas condiciones, es decir, una dilución 1 en 100 de sangre con oxalato de amonio tal como mencionamos anteriormente utilizando solo 5 cuadrados medianos del cuadrado central.Necesitamos el volumen donde están las plaquetas, el volumen resulta al multiplicar la superficie por la altura, la superficie de cada cuadrado, mediano es de 0.04mm2 y la sumatoria de los 5 cuadrados medianos es de 0.2mm2, la altura de hematímetro hasta el cubrehematímetro es de 0.1mm entonces, 0.2mm2 x 0.1mm = 0.02mm3 esto sería el volumen total de cuando se observa en el microscopio las plaquetas.
En el primer cuadrado mediano contamos 8 plaquetas, en el segundo 9, en el tercero 12, cuarto 9 y el quinto 10 plaquetas sumando nos da en total de 48 plaquetas. Ahora toca calcular el factor de estándar bajo estas condiciones para el recuento de plaquetas:
Si N plaquetas ____________________se contaron en un volúmen total de 0,02mm3
X plaquetas habrán ____________________________ En un volúmen de 1mm3?
Número de plaquetas /mm3=(1〖mm〗^3 x N células )/(0,02〖mm〗^3 ) x dilución(100)
Multiplicamos lo siguiente para hallar el factor: 1mm3 x dilución (100) entre volumen (0.02mm3)
Número de plaquetas /〖mm〗^3= 5 000
Entoces el factor es 5 000; ahora para hallar el recuento total de plaquetas multiplicamos el factor con el número de plaquetas contadas(N).
Número de plaquetas/〖mm〗^3=5 000 x 48 Obtenimos 240, 000 plaquetas por mm3 o es lo mismo decir (240, 000 plaq/uL) (1)
CAPÍTULO IV
CÁMARA DE NEUBAUER PARA EL RECUENTO DE LEVADURAS
Se realiza para saber la viabilidad y tiraje de las levaduras usando formulas correspondientes Homogeneizar la suspensión de levaduras cuyo recuento se pretende determinar. Depositar sobre la cuadricula de la cámara 2 gotas de suspensión. Cubrir la cámara con el cubreobjetos con cuidado de no producir burbujas de aire. No es necesario contar los 256 cuadraditos, se van a contar 5 grupos (cuadrados) de 16 cuadraditos en áreas diferentes de la cámara.Cuadro grande central (centro de la cruz, 400 cuadros pequeños): 1mm /400 cuadros.
Cuadro mediano (formado por 5x5=25 cuadros pequeños): 0.25 mm x 0.25 mm Cuadro pequeño: 0.05 mm x 0.05 mm = 0.0025 mm Líneas separadoras de cuadros medianos (en rojo): 0.025 mm del extremo del cuadro pequeño Datos básicos (mismas medidas que las anteriores excepto cuadro mediano) :/400 cuadros. = 0.0025 mm El enfoque del microscopio se empieza con el objetivo de menor aumento que posteriormente pasaremos a uno de más. Se centra el objetivo del microscopio a ojo en el centro teórico de la cruz de la cámara, luego se coloca el objetivo lo más cerca posible del cubre objetos, pero sin tocarlo y posteriormente se irá alejándolo hasta que la imagen sea lo más clara y nítida posible. Se aconseja trabajar a 400 aumentos. Contabilizar levaduras totales: Se aconseja siempre hacer la media de levaduras contenidas en varios grupos de cuadros. Por ejemplo, se presenta contabilizar las levaduras contenidas en los grupos de 25 y 16 cuadros respectivamente según la cámara usada.2/5
cálculos para producción de cerveza
• 1º - Sumar el número de células contadas.
• 2º - Multiplico para obtener cuántas células hay en un volumen final de 1 mL
• 3º - Multiplico por la dilución realizada
Ejemplo:
Si la suma de 5 cuadrados da un total de 300
entonces el total de la cámara (estimado) será de
300 x 5 = 1.500
Las células por ml se estiman en:
1.500 x 10.000 = 15.000.000 = 1,5 x 107
Multiplico por factor de dilución ejemplo (1/100)
entonces:
1,5 x 107 x 100 = 1,5 x 109 (billones) (2)
Métodos de recuento de levaduras:
Se colocan 400 µL de muestra homogenizada en un microtubo y se añaden 40 µL de azul de Evans o azul de metileno fenicado. La muestra y el colorante se mezclan y se dejan en reposo a temperatura ambiente durante 5 min. Se deposita una gota en una de las 2 cuadrículas del portaobjetos procurando que quede llena la superficie y se tapa con el cubreobjetos evitando la presencia de burbujas de aire. La cámara de recuento se ha de fijar en la platina del microscopio para realizar la observación microscópica. El enfoque del microscopio se empieza con un objetivo de pocos aumentos que posteriormente pasaremos a uno de más. Se coloca el objetivo lo más cerca posible del cubreobjetos, pero sin tocarlo y posteriormente se irá alejando hasta que la imagen sea lo más clara y nítida posible. Sea cual fuese el modelo de cámara empleado, el procedimiento es el mismo, el recuento se realizará sobre 20 de los 400 (20 x 20) cuadrados pequeños de 0,0025 mm2 (volumen total de 0,1 mm3) elegidos al azar. Si el número de células/cuadrado es >10 es conveniente diluir la muestra. Detalle del cuadrado de la cámara de recuento de Thoma, Por convenio para evitar contar dos veces la misma levadura, consideraremos que las levaduras que se encuentren en la intersección de una cuadrícula se apuntarán a la de abajo y a la de la izquierda, y las gemaciones se cuentan como 1/2 levadura. Las levaduras vivas se pueden diferenciar de las muertas porque el azul de Evans colorea las células viables mientras que el azul de metileno sólo colorea las no viables.
Sea n el número total de levaduras en las 20 cuadrículas. (3)
CAPÍTULO V
RECUENTO DE ESPERMATOZOIDES EN CÁMARA DE NEUBAUER
Realizar una investigación inicial, la estimación de la concentración, es importante que la cantidad de semen depositado y el tamaño del cubreobjeto, utilizado sea siempre los mismos para que todos los exámenes se realicen en una preparación del mismo espesor, (20uL) esto permite el cálculo aproximado de la concentración de los espermatozoides, para poder determinar la dilución.Un volumen fijo de 10uL de semen es depositado en un portaobjeto utilizando una pipeta de desplazamiento positivo y cubierto con un cubreobjeto de 22 x 22 mm. El peso de esta distribuye la muestra para una visión optima. Luego se debe permitir a que se estabilice durante 1 minuto, dado que la motilidad y la vitalidad de los espermatozoides es dependiente a la temperatura. La evaluación inicial con una magnificación de 100x, por ejemplo, 10 x objetivo y 10 x ocular. Se realiza la estimación preliminar de la concentración espermática en una profundidad de 20um, explorando el portaobjeto y estimando el número de espermatozoides por campo, o por parte de un campo equivale a 1nL se obtiene la concentración aproximada de espermatozoides en 106/mL. Esta estimación es utilizada para decidir la dilución a utilizar en la determinación de la concentración de espermatozoides en el hemocitómetro o cámara de Neubauer.
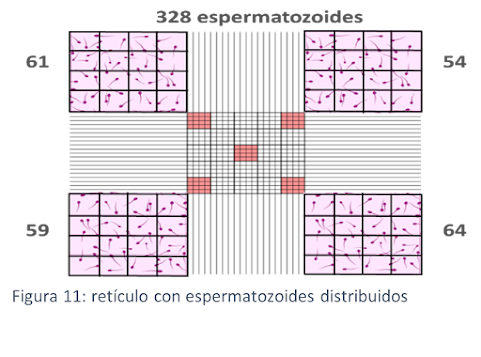
Para este caso se hizo una dilución en un tubo de ensayo en donde se agregó 50uL de semen y 950 de diluyente, por lo que el volumen total de la dilución es 1000 que es lo mismo una dilución 1/20 el diluyente cumple lo siguiente, colorea a los espermatozoides y las mata, luego disponemos la cámara de Neubauer y con ayuda de una pipeta automática cargamos la dilución, para llevar al microscopio con el objetivo de 10x enfocamos los campos luego con 40x hacer el recuento. El recuento se realiza los 4 cuadrados de la esquina del retículo.
Se contaron lo siguiente: 61, 54, 59 y 64 espermatozoides respectivamente de tal forma que se obtuvo un total de 238/4cuadrados, pasamos a sacar el promedio de espermatozoides que es 59,5cel/cuadrado. (4)
Se contaron lo siguiente: 61, 54, 59 y 64 espermatozoides respectivamente de tal forma que se obtuvo un total de 238/4cuadrados, pasamos a sacar el promedio de espermatozoides que es 59,5cel/cuadrado. (4)
Aplicamos la fórmula:
1- Relativa imprecisión inherente al método. Estadísticamente el error sigue una distribución de Poisson, y su varianza es dependiente del número de células contadas, siendo menor a medida que aumenta su número.
2- Requerimiento de personal cualificado. Necesidad de un período de aprendizaje variable (curvas de aprendizaje). Presenta una elevada imprecisión Inter observador. 3- Consumo de recursos elevado.
Al tratarse de un método manual, y requerir varios pasos para su realización, los costes de personal elevan el gasto asociado al mismo. En los últimos años se han propuesto sistemas automatizados de recuento celular con objeto de facilitar este proceso analítico. La tecnología de los contadores hematológicos automáticos con una combinación de las técnicas de impedancia, ópticas y citometría de flujo, aplicadas al hemograma, puede resultar de gran ayuda para el estudio de los líquidos biológicos, aumentando la fiabilidad, con disminución de la imprecisión y del tiempo requerido para su realización. Recuento Eritrocitario Proporciona escasa información diagnóstica. Su origen es sanguíneo y la presencia de 5.000-10.000 hematíes / mm3 es suficiente para dar una coloración rojiza hemática al líquido. Es más frecuente en exudados que en trasudados.
En líquidos con recuento eritrocitario mayor de 100.000 hematíes/mm3 se debe determinar el valor hematocrito del mismo, y en caso de ser superior al 50 % del equivalente sanguíneo, será diagnóstico de hemotórax en caso de líquido pleural. Si la presencia de sangre es debida a la toracocentesis, se observará un aclaramiento progresivo de la colección durante la obtención del líquido. Los líquidos hemorrágicos se han asociado con infecciones paraneumónicas, neoplasias, conectivopatías, asbestosis, enfermedades abdominales (pancreatitis, síndrome de Meigs, pleuritis urémica), origen cardiovascular (rotura de aneurisma, infarto pulmonar, tromboembolismo, bypass aorto coronario), trastornos de la coagulación (sobredosis de anticoagulación, microangiopatías, cirrosis hepática), insuficiencia renal crónica y otras. Recuento leucocitario Su utilidad diagnóstica es limitada. La mayoría de los líquidos trasudados tienen una concentración inferior a 1.000 leucocitos / mm3, mientras que en la mayoría de los exudados la cifra es superior a 1.000 leucocitos / mm3. Concentraciones superiores a 10.000 leucocitos / mm3 son sugestivas de derrame paraneumónico, tuberculosis, pancreatitis, neoplasias, síndrome postinfarto, o Lupus Eritematoso Sistémico (LES). Concentraciones superiores a 50.000 leucocitos /mm3 sugieren pancreatitis o un embolismo pulmonar. Es recomendable efectuar fórmula leucocitaria cuando la concentración de leucocitos es superior a 250 /mm3. Los porcentajes de los diferentes tipos de leucocitos observados en el líquido pleural van a ser sugerentes de uno u otro diagnóstico. Así, un porcentaje de polimorfonucleares neutrófilos > 50 % orienta hacia un proceso agudo, generalmente de carácter inflamatorio, neumonía aguda, pancreatitis, tromboembolismo pulmonar (TEP), asbestosis, LES, absceso subfrénico, fase inicial de tuberculosis y en algunas neoplasias en fase precoz. Por el contrario, un porcentaje de mononucleares > 50 % orienta hacia un proceso crónico. La presencia de linfocitos de pequeño tamaño sugiere etiología neoplásica o tuberculosa. Otras causas son quilotórax, artritis reumatoidea, linfomas, y sarcoidosis. Un Porcentaje de eosinófilos > 10 % de eosinófilos (derrame eosinófilo) se observa en casos de hemotórax, neumotórax (aire en el espacio pleural). Otras causas posibles podrían ser toracocentesis repetidas, reacciones a fármacos, asbestosis, síndrome de Churg-Strauss, enfermedad de Hodgkin, y enfermedades parasitarias (hidatidosis, amebiasis o ascaridiasis). La presencia de basófilos en el líquido pleural es infrecuente y cuando el porcentaje es superior al 10 % se asocia con leucemias con afectación pleural. Otras células
• Macrófagos Su origen son los monocitos circulantes. Son de limitada utilidad diagnóstica, es importante no confundirlas con células neoplásicas.
• Células mesoteliales: Su presencia indica afectación pleural difusa, y orienta hacia derrames tuberculosos, paraneumónico complicados y neoplásicos.
• Células plasmáticas Su presencia en el líquido pleural orienta hacia el diagnóstico de un mieloma múltiple.
• Células cancerosas El análisis citológico de células cancerosas tiene una sensibilidad diagnóstica del 60 % para una única muestra en los derrames carcinomatosos, siendo únicamente del 30 % para el caso del mesotelioma. La sensibilidad aumenta si se toman una segunda y tercera muestras. (5)
Procedimiento de recuento celularidad en Liquido Céfalo Raquídeo
En un tubo de ensayo colocar 10uL de colorante cristal violeta al 0.2%
Agregar 90ul de fluido biológico previamente homogenizado y dejar que actúe el colorante
Cargar en la cámara de Neubauer aprox. 10uL de la solución coloreada dejar reposar 5 minutos para luego realizar el recuento.
Se contabiliza los leucocitos en los 9 cuadrados del retículo
El número de leucocitos total por mm3 es igual al número de leucocitos en los 9 cuadrados multiplicado por 1.23.
El 1.23 se obtiene de la siguiente manera:
Área del retículo = ancho por largo
Área de retículo = 3mm x 3mm = 9mm2
Volumen leído = 9mm2 x 0.1mm = 0.9mm3
Para obtener el número de leucocitos en 1mm3, se busca un número que multiplicado por 0.9mm3 nos resulte 1mm3
1/0.9 = 1.11
0.9mm3 x 1.11 = 1mm3
Según la fórmula:
N° Leucocitos /mm3 = leucocitos contados x título de dilución x N° Encontrados
N° Leucocitos /mm3 = leucocitos encontrados x 10/9 x1.11
N° Leucocitos /mm3 = leucocitos encontrados x 1.23
Con esta fórmula se encuentra el número real de leucocitos por mm3. En caso de fluidos biológicos Turbios, con pleocitosis marcada con elementos celulares iguales o mayor que en sangre, para el recuento emplearan las mismas diluciones que en hematología. Es decir, diluyendo la muestra (1/10, 1/20) con liquido de Turk. El número de leucocitos contados en los cuadrantes se multiplica por 25 0 50 según su dilución empleada. En caso de otros fluidos que son purulentos que se coagulan con facilidad y no tienen heparina (líquido pleural, sinovial, etc.) se recomienda usar el suero fisiológico como dilución, esto evitara su coagulación de la muestra y permite realizar un buen recuento celular. Se debe realizar un examen directo en fresco para informar el porcentaje de leucocitos aglutinados, porcentaje de leucocitos aglutinados si lo hubiera, presencia de detritus celular hematíes por campo, etc. Cuando el fluido biológico es hemorrágico o ligeramente hemático, antes de realizar el recuento citológico se hará un examen directo en fresco (se recomienda sin cubre objeto) para reportar hematíes por campo porcentaje de crenados si lo hubiera. Este dato es importante sobre todo en LCR.
CAPÍTULO VI
EXÁMEN MICROSCÓPICO DE LÍQUIDOS BIOLÓGICOS
Estudio celular Fisiológicamente el líquido biológico contiene escasa celularidad, siendo ésta predominantemente de macrófagos (75%), linfocitos (23 %), y células mesoteliales (2%). Las células presentes en el líquido biológicos pueden ser de origen sanguíneo (hematíes y leucocitos), o de orígenes diferentes. Recuento celular: Diversos estudios han mostrado que no existen diferencias estadísticamente significativas en recuentos efectuados hasta 24 horas post-extracción del espécimen, cuando éste se conserva a 4ºC Es importante estandarizar el tipo de anticoagulación que se establece para conservar el líquido, siendo el contenedor más adecuado el tubo anticoagulado con EDTA. No es aconsejable recoger el espécimen en un tubo sin anticoagulante Tradicionalmente el recuento se ha realizado en cámara hematocitométrica (Neubauer, Burker o Thoma), similar a las usadas en los recuentos hematológicos manuales. Esta forma de recuento presenta una serie de características:1- Relativa imprecisión inherente al método. Estadísticamente el error sigue una distribución de Poisson, y su varianza es dependiente del número de células contadas, siendo menor a medida que aumenta su número.
2- Requerimiento de personal cualificado. Necesidad de un período de aprendizaje variable (curvas de aprendizaje). Presenta una elevada imprecisión Inter observador. 3- Consumo de recursos elevado.
Al tratarse de un método manual, y requerir varios pasos para su realización, los costes de personal elevan el gasto asociado al mismo. En los últimos años se han propuesto sistemas automatizados de recuento celular con objeto de facilitar este proceso analítico. La tecnología de los contadores hematológicos automáticos con una combinación de las técnicas de impedancia, ópticas y citometría de flujo, aplicadas al hemograma, puede resultar de gran ayuda para el estudio de los líquidos biológicos, aumentando la fiabilidad, con disminución de la imprecisión y del tiempo requerido para su realización. Recuento Eritrocitario Proporciona escasa información diagnóstica. Su origen es sanguíneo y la presencia de 5.000-10.000 hematíes / mm3 es suficiente para dar una coloración rojiza hemática al líquido. Es más frecuente en exudados que en trasudados.
En líquidos con recuento eritrocitario mayor de 100.000 hematíes/mm3 se debe determinar el valor hematocrito del mismo, y en caso de ser superior al 50 % del equivalente sanguíneo, será diagnóstico de hemotórax en caso de líquido pleural. Si la presencia de sangre es debida a la toracocentesis, se observará un aclaramiento progresivo de la colección durante la obtención del líquido. Los líquidos hemorrágicos se han asociado con infecciones paraneumónicas, neoplasias, conectivopatías, asbestosis, enfermedades abdominales (pancreatitis, síndrome de Meigs, pleuritis urémica), origen cardiovascular (rotura de aneurisma, infarto pulmonar, tromboembolismo, bypass aorto coronario), trastornos de la coagulación (sobredosis de anticoagulación, microangiopatías, cirrosis hepática), insuficiencia renal crónica y otras. Recuento leucocitario Su utilidad diagnóstica es limitada. La mayoría de los líquidos trasudados tienen una concentración inferior a 1.000 leucocitos / mm3, mientras que en la mayoría de los exudados la cifra es superior a 1.000 leucocitos / mm3. Concentraciones superiores a 10.000 leucocitos / mm3 son sugestivas de derrame paraneumónico, tuberculosis, pancreatitis, neoplasias, síndrome postinfarto, o Lupus Eritematoso Sistémico (LES). Concentraciones superiores a 50.000 leucocitos /mm3 sugieren pancreatitis o un embolismo pulmonar. Es recomendable efectuar fórmula leucocitaria cuando la concentración de leucocitos es superior a 250 /mm3. Los porcentajes de los diferentes tipos de leucocitos observados en el líquido pleural van a ser sugerentes de uno u otro diagnóstico. Así, un porcentaje de polimorfonucleares neutrófilos > 50 % orienta hacia un proceso agudo, generalmente de carácter inflamatorio, neumonía aguda, pancreatitis, tromboembolismo pulmonar (TEP), asbestosis, LES, absceso subfrénico, fase inicial de tuberculosis y en algunas neoplasias en fase precoz. Por el contrario, un porcentaje de mononucleares > 50 % orienta hacia un proceso crónico. La presencia de linfocitos de pequeño tamaño sugiere etiología neoplásica o tuberculosa. Otras causas son quilotórax, artritis reumatoidea, linfomas, y sarcoidosis. Un Porcentaje de eosinófilos > 10 % de eosinófilos (derrame eosinófilo) se observa en casos de hemotórax, neumotórax (aire en el espacio pleural). Otras causas posibles podrían ser toracocentesis repetidas, reacciones a fármacos, asbestosis, síndrome de Churg-Strauss, enfermedad de Hodgkin, y enfermedades parasitarias (hidatidosis, amebiasis o ascaridiasis). La presencia de basófilos en el líquido pleural es infrecuente y cuando el porcentaje es superior al 10 % se asocia con leucemias con afectación pleural. Otras células
• Macrófagos Su origen son los monocitos circulantes. Son de limitada utilidad diagnóstica, es importante no confundirlas con células neoplásicas.
• Células mesoteliales: Su presencia indica afectación pleural difusa, y orienta hacia derrames tuberculosos, paraneumónico complicados y neoplásicos.
• Células plasmáticas Su presencia en el líquido pleural orienta hacia el diagnóstico de un mieloma múltiple.
• Células cancerosas El análisis citológico de células cancerosas tiene una sensibilidad diagnóstica del 60 % para una única muestra en los derrames carcinomatosos, siendo únicamente del 30 % para el caso del mesotelioma. La sensibilidad aumenta si se toman una segunda y tercera muestras. (5)
Procedimiento de recuento celularidad en Liquido Céfalo Raquídeo
En un tubo de ensayo colocar 10uL de colorante cristal violeta al 0.2%
Agregar 90ul de fluido biológico previamente homogenizado y dejar que actúe el colorante
Cargar en la cámara de Neubauer aprox. 10uL de la solución coloreada dejar reposar 5 minutos para luego realizar el recuento.
Se contabiliza los leucocitos en los 9 cuadrados del retículo
El número de leucocitos total por mm3 es igual al número de leucocitos en los 9 cuadrados multiplicado por 1.23.
El 1.23 se obtiene de la siguiente manera:
Área del retículo = ancho por largo
Área de retículo = 3mm x 3mm = 9mm2
Volumen leído = 9mm2 x 0.1mm = 0.9mm3
Para obtener el número de leucocitos en 1mm3, se busca un número que multiplicado por 0.9mm3 nos resulte 1mm3
1/0.9 = 1.11
0.9mm3 x 1.11 = 1mm3
Según la fórmula:
N° Leucocitos /mm3 = leucocitos contados x título de dilución x N° Encontrados
N° Leucocitos /mm3 = leucocitos encontrados x 10/9 x1.11
N° Leucocitos /mm3 = leucocitos encontrados x 1.23
Con esta fórmula se encuentra el número real de leucocitos por mm3. En caso de fluidos biológicos Turbios, con pleocitosis marcada con elementos celulares iguales o mayor que en sangre, para el recuento emplearan las mismas diluciones que en hematología. Es decir, diluyendo la muestra (1/10, 1/20) con liquido de Turk. El número de leucocitos contados en los cuadrantes se multiplica por 25 0 50 según su dilución empleada. En caso de otros fluidos que son purulentos que se coagulan con facilidad y no tienen heparina (líquido pleural, sinovial, etc.) se recomienda usar el suero fisiológico como dilución, esto evitara su coagulación de la muestra y permite realizar un buen recuento celular. Se debe realizar un examen directo en fresco para informar el porcentaje de leucocitos aglutinados, porcentaje de leucocitos aglutinados si lo hubiera, presencia de detritus celular hematíes por campo, etc. Cuando el fluido biológico es hemorrágico o ligeramente hemático, antes de realizar el recuento citológico se hará un examen directo en fresco (se recomienda sin cubre objeto) para reportar hematíes por campo porcentaje de crenados si lo hubiera. Este dato es importante sobre todo en LCR.
Referencias Bibliográficas
1. Sonnenwirth AC, Jarett L. TÉCNICAS MANUALES. In Daniel Landes CAG, editor. Métodos y Diagnósticos del Laboratorio Clínico. 8th ed. Buenos Aires: Editorial Médica Panamericana; 1986. p. 727-734.
2. Moliné DLCTM. Inibioma Conicet Unco. [Online].; Argentina 2014 [cited 2019 Noviembre 08. Available from: http://www.somoscerveceros.com/wp-content/uploads/2014/Teorica-curso-micorscopico-la-plata-2014-V5.pdf.
3. Sáez PB. Urbina Vinos Blog. [Online].; 2015 [cited 2019 Noviembre 02. Available from: http://urbinavinos.blogspot.com/2015/04/recuento-de-levaduras-en-enologia.html.
4. SALUD OMDL. Manual de laboratorio de la OMS para el examen de Semen Humano y de la interaccion entre el semne y el moco cervical. 4th ed. BLAQUIER DJAByCM, editor. España: EDITORIAL MEDICA PANAMERICANA S.A.; 2001.
5. Izquierdo F. Líquidos biológicos: actualización del análisis en el laboratorio. [Online].; 2010 [cited 2019 Noviembre 12. Available from: https://www.researchgate.net/publication/235798871.
6. STUDYLIB.ES. STUDYLIB.ES. [Online].; 2013 [cited 2019 Noviembre 02. Available from: https://studylib.es/doc/5759001/recuento-de-levaduras.